EM 313 – TERMODINÂMICA I
2A PROVA
1A QUESTÃO
1
kg de água executa um ciclo de potência de Carnot. Durante o processo de
expansão isotérmica, a água é aquecida até o estado de vapor saturado a partir
de um estado inicial onde a pressão é 15 bar e o título igual a zero. O vapor é
então expandido até a pressão de 1 bar e título de 84,9%.
a)
Mostre o ciclo
num diagrama P-v
b)
Calcule o calor e
o trabalho para cada processo, em kJ
c)
Calcule a
eficiência térmica
Resolução
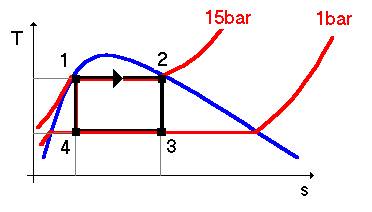
Ciclo de Carnot:
a)
processos
reversíveis;
b)
processos
adiabáticos e reversíveis são isentrópicos;
c)
s1=s3;
d)
s2=s4.
|
Estado 1 |
Estado 2 |
Estado 3 |
Estado 4 |
|
|
Pressão (bar) |
15 |
15 |
1 |
1 |
|
Título |
0 |
1 |
0,849 |
0,167 |
|
Temp. (°C) |
198,32 |
198,32 |
99,63 |
99,63 |
|
Temp. (K) |
471,47 |
471,47 |
372,78 |
372,78 |
|
u (kJ/kg) |
843,17 |
2594,5 |
2190,7 |
766,48 |
|
s (kJ/kgK) |
2,315 |
6,4448 |
6,4448 |
2,315 |
Primeira Lei da Termodinâmica para sistemas:
U2 –
U1 = Q12 – W12
Para o processo 1-2:
Q12 =
m( T1 )( S2-S1 ) = 1947,1 kJ
Para o processo 3-4:
Q34 =
m( T3 )( S4-S3 ) = -1539,5 kJ
U2 –
U1 = Q12 – W12
W12
= Q12 - U2 + U1 = 195,8 kJ
U4 –
U3 = Q34 – W34
W34
= Q34 – U4 + U3 = -114,8 kJ
Os processos 2-3 e 4-1 são adiabáticos:
Q23 = 0 e Q41 = 0
U3 –
U2 = Q23 – W23
W23
= Q23 – U3 + U2 = 403,8 kJ
U1 –
U4 = Q41 – W41
W41
= Q41 – U4 + U1 = -76,7 kJ
O rendimento térmico do ciclo pode ser calculado por
Rt = 1 - T1/T3
= 1 – 372,8/471,5 = 0,209
Pode ser também calculado por
Rt = Wciclo/Q12 = 407,6/1947,8 = 0,209
2A QUESTÃO
Um conjunto cilindro-pistão inicialmente contém 0,1 m³ de CO2
a 0,3 bar e 400 K. O gás é comprimido isoentropicamente até um estado onde a
temperatura é 560 K. Utilizando o modelo do gás ideal e desprezando as
variações de energia cinética e potencial, determine a pressão final, em bar, e
o trabalho, em kJ, utilizando:
a)
calor específico
variável
b)
calor específico
constante a 480 K
Resolução
Compressão isentrópica
|
|
Estado 1 |
Estado 2(a) |
Estado 2(b) |
|
Volume (m3) |
0,1 |
0,1 |
|
|
Pressão (kPa) |
0,3 |
176,43 |
177,96 |
|
Temp. (K) |
400 |
560 |
560 |
(b) calor específico constante a 480 K
cp(molar) = 43,991 kJ/(kmol K)
processo isentrópico s2=s1
s2-s1=cp
ln(T2/T1) – Runiv ln(p2/p1)
= 0
ln(p2/p1)
= 1,78034
p2 =
177,96 kPa
Pela 1a. Lei da Termodinâmica:
W12
= U1 – U2 = n cv(molar) (T1-T2)
W12
= - (9,021/1000) 35,677 (160)
W12
= - 5,149 kJ
(a) calor específico variável
Tabela de gases:
so(560)=
26,25 kJ/(kmolK)
so(400)=
11,52 kJ/(kmolK)
processo isentrópico s2=s1
s2-s1=
26,25 – 11,52 – Runiv ln(p2/p1) = 0
ln(p2/p1)
= 1,77171
p2 =
176,43 kPa
Pela 1a. Lei da Termodinâmica:
W12
= U1 – U2 = n (u1 – u2)
W12 = (9,021/1000) (675,4 – 6373,9) kJ
W12 = - 5,141 kJ
3A QUESTÃO
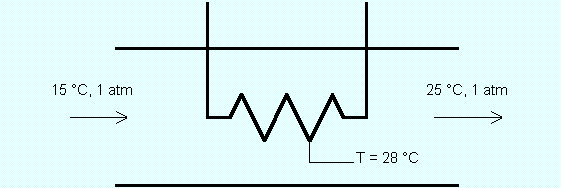
A figura abaixo mostra uma resistência elétrica de 30 W localizada em um duto isolado por onde escoa uma corrente
de ar. Em regime permanente, uma corrente de 15 A passa pela resistência, cuja
temperatura se mantém constante em 28 °C. O ar entra no duto a 15 °C, 1
atm e sai a 25 °C na mesma pressão.
Desprezar as variações de energia cinética e potencial.
a)
Para a
resistência como sistema, calcule a geração de entropia, em kW/K
b)
Para um volume de
controle que inclua o ar no duto e a resistência, determine a descarga de ar,
em kg/s, e a taxa de geração de entropia, em kW/K
Resolução
(a) para a resistência como sistema
Há entrada de potência elétrica: Wel = - R I2
= - 30 (15)2 = - 6,75 kW
Há transferência de calor para o exterior do sistema: Q = Wel=
- 6,75 kW
A geração de entropia no interior do sistema:
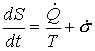
![]()
(b) para o duto considerado como volume de controle
|
|
Entrada |
Saída |
|
Temperatura (°C) |
15 |
25 |
|
Pressão (atm) |
1 |
1 |
![]()
![]()
![]()
![]()
Para o balanço de entropia no volume de controle:
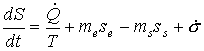
![]()
![]()
A geração de entropia é maior neste caso pois inclui a irreversibilidade
associada à transferência de calor entre a resistência e o ar.